注意!6月1日起,这些医疗器械需具有医疗器械唯一标识
来源:医美达日期:2024-05-14阅读39
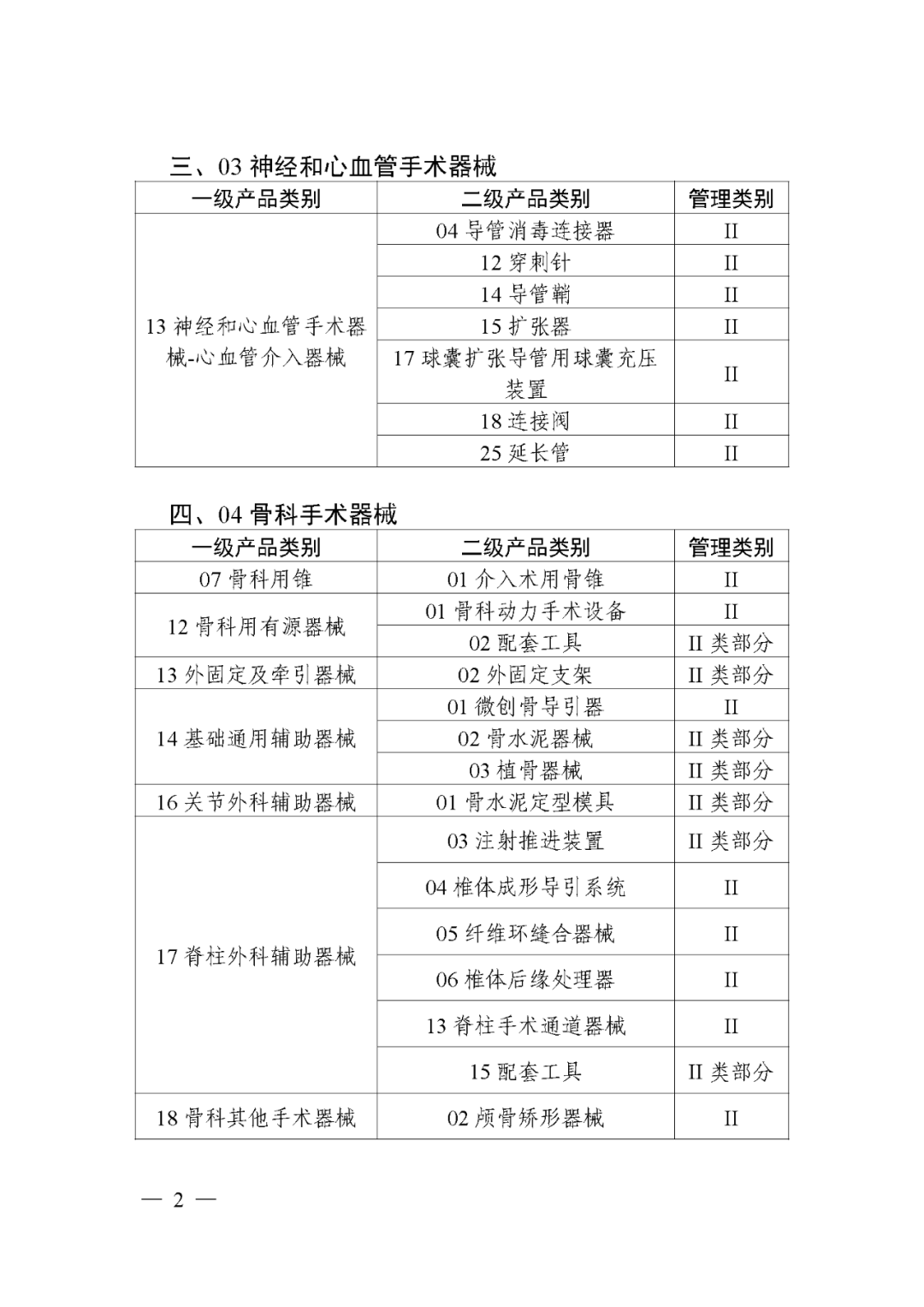
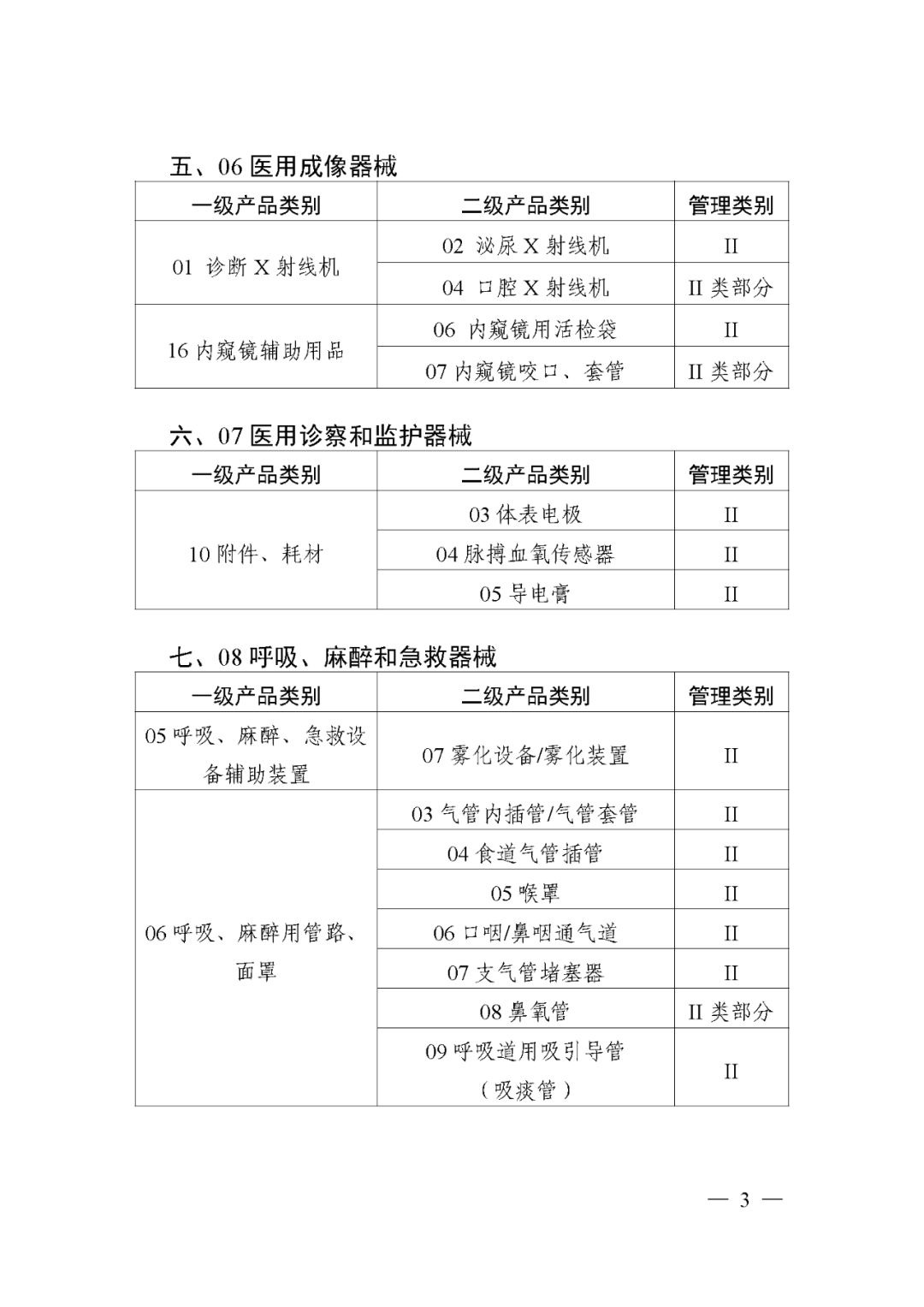
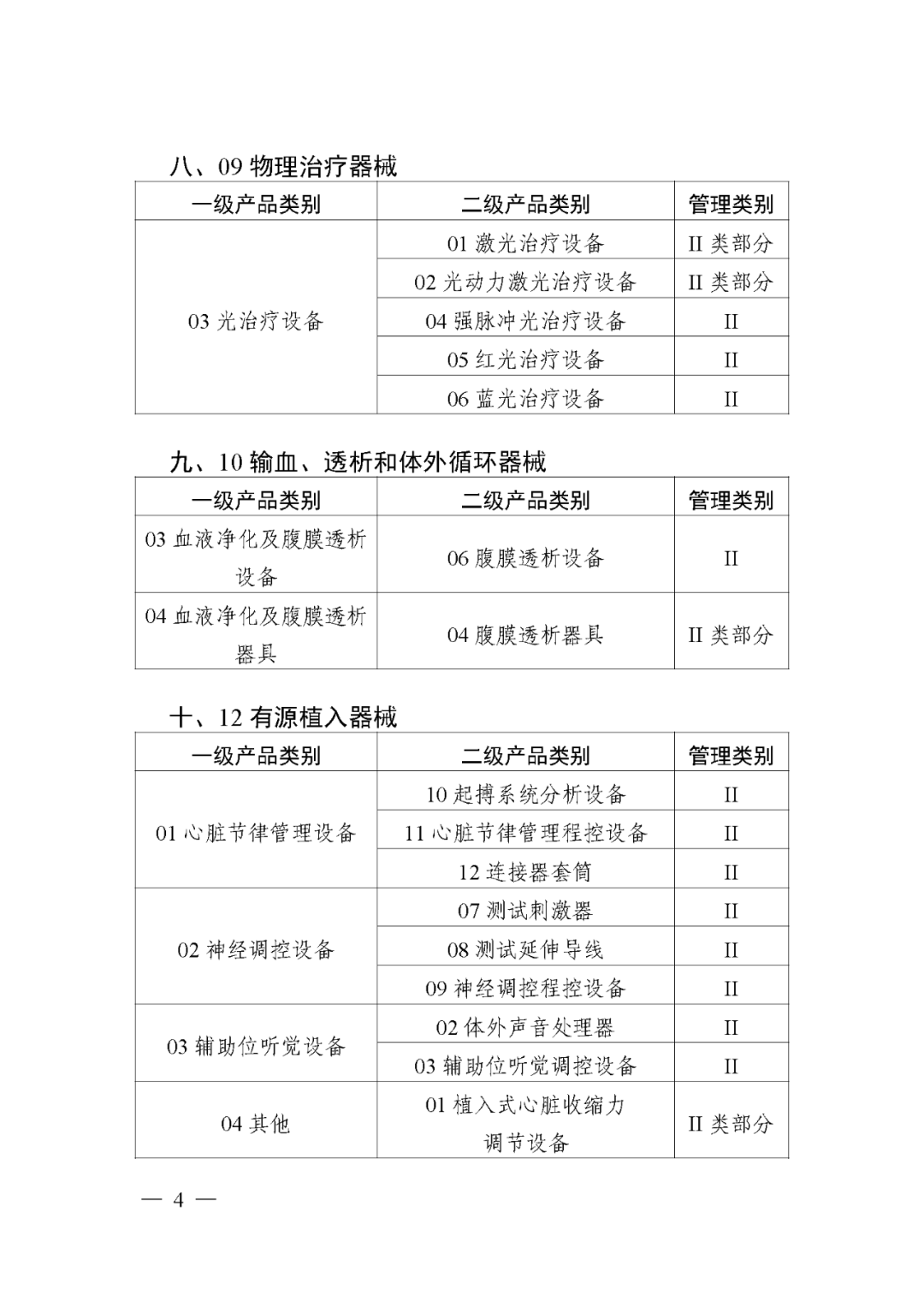
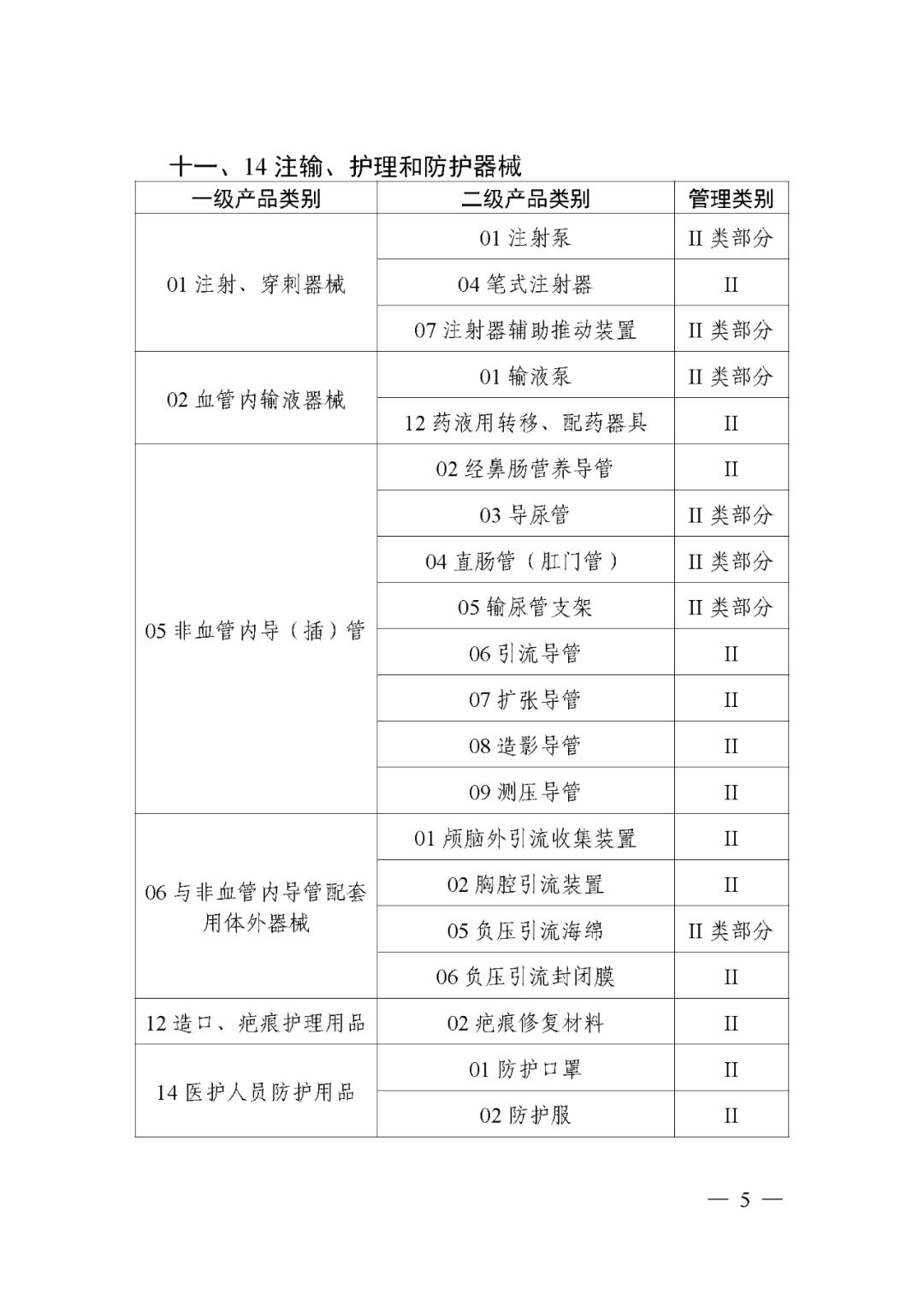
据国家药监局官网于2023年2月17日发布的公告显示,自2024年6月1日起,被列入第三批实施产品目录的103个第二类医疗器械(见文末)实施医疗器械唯一标识。
1、2024年6月1日起生产的医疗器械应当具有医疗器械唯一标识。
2、2024年6月1日起申请注册的,注册申请人应当在注册管理系统中提交其产品最小销售单元的产品标识。
产品标识不属于注册审查事项,产品标识的单独变化不属于注册变更范畴。
3、2024年6月1日起生产的医疗器械,在其上市销售前,注册人应当按照相关标准或者规范要求将最小销售单元、更高级别包装的产品标识和相关数据上传至医疗器械唯一标识数据库,确保数据真实、准确、完整、可追溯。
当医疗器械最小销售单元产品标识相关数据发生变化时,注册人应当在产品上市销售前,在医疗器械唯一标识数据库中进行变更,实现数据更新。医疗器械最小销售单元产品标识变化时,应当按照新增产品标识在医疗器械唯一标识数据库上传数据。
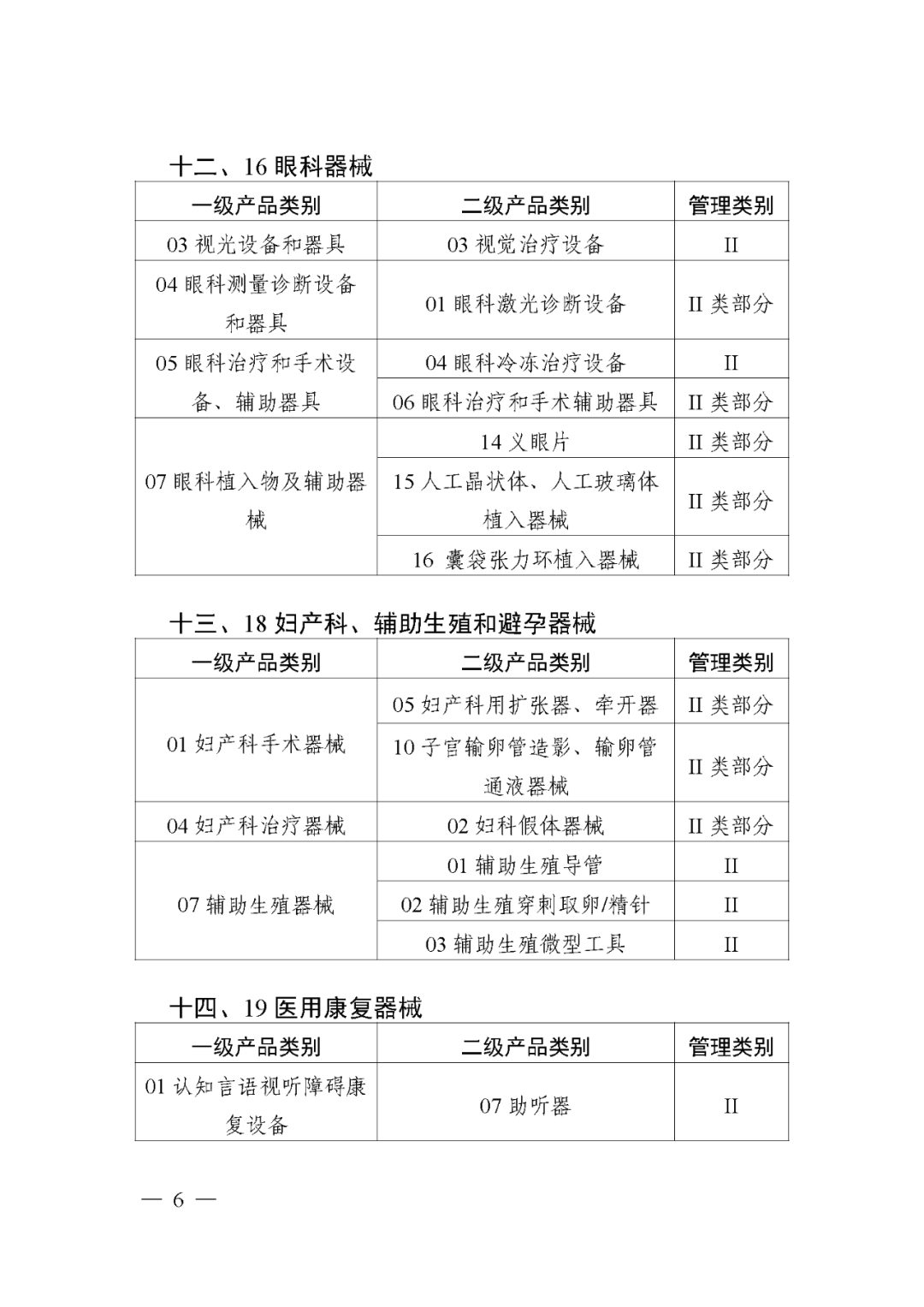
第三批实施医疗器械唯一标识的产品目录