美国FDA UDI 12月8日强制执行,仅剩30天
来源:医美达日期:2022-11-08阅读215
美国UDI要求:
美国目前要求所有设备都符合标签和数据库要求,FDA要求所有的UDI信息都必须输入美国特定的GUDID数据库。
2022年12月8日之后,对I类和非分类设备(植入式、支持生命或维持生命的设备(I/LS/LS)除外)实施FDA GUDID提交要求,无论其是否为消费者健康产品(Consumer Health Products)。
美国UDI合规时间表
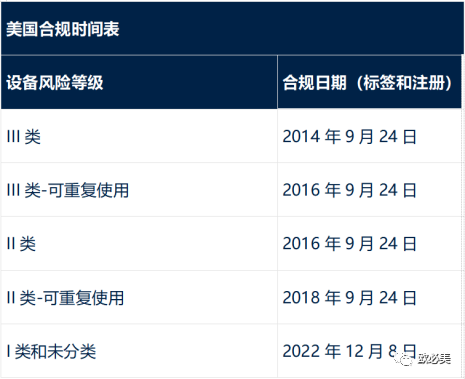
所有医疗器械产品向FDA GUDID注册产品数据;
产品包装具备UDI载体。
医美达能为您做什么:
帮助您确认UDI前期准备资料;
GUDID数据库账户创建;
产品UDI信息输入GUDID数据库等。
什么是UDI?
唯一设备标识符(UDI)现在是在美国销售的医疗设备的一项要求,并且已逐步被欧盟和其他国家采用。UDI系统旨在为医疗保健用品提供者、制造商、授权的卫生当局、医院和机构以及个人消费者提供:
●卫生部门更快地发现可能存在缺陷的医疗器械信息。
● 更快地访问召回信息,并查看当前库存。
● 通过一致记录的产品有效期减少医疗差错。
● 识别医疗设施中使用的任何假冒产品。
● 保证有关植入设备的信息是安全保留和可追踪的。
UDI的时间表和截止日期因市场和产品而异,在一些国家已多次修订。
UDI要求有两个主要组件,标签和数据库注册。尽管努力协调各市场的标签和数据库要求,但有UDI采用计划的国家增加了针对市场的要求。
目前实行UDI要求的国家/地区有:
· 澳大利亚UDI
· 巴西UDI
· 加拿大UDI
· 中国UDI
· 欧盟UDI
· 印度UDI
· 日本UDI
· 沙特阿拉伯UDI
· 新加坡UDI
· 韩国UDI
· 台湾UDI
· 美国UDI







