6月1日起,唯一标识覆盖所有三类医疗器械,无编码不采购
来源:医美达日期:2022-05-31阅读400
导 言
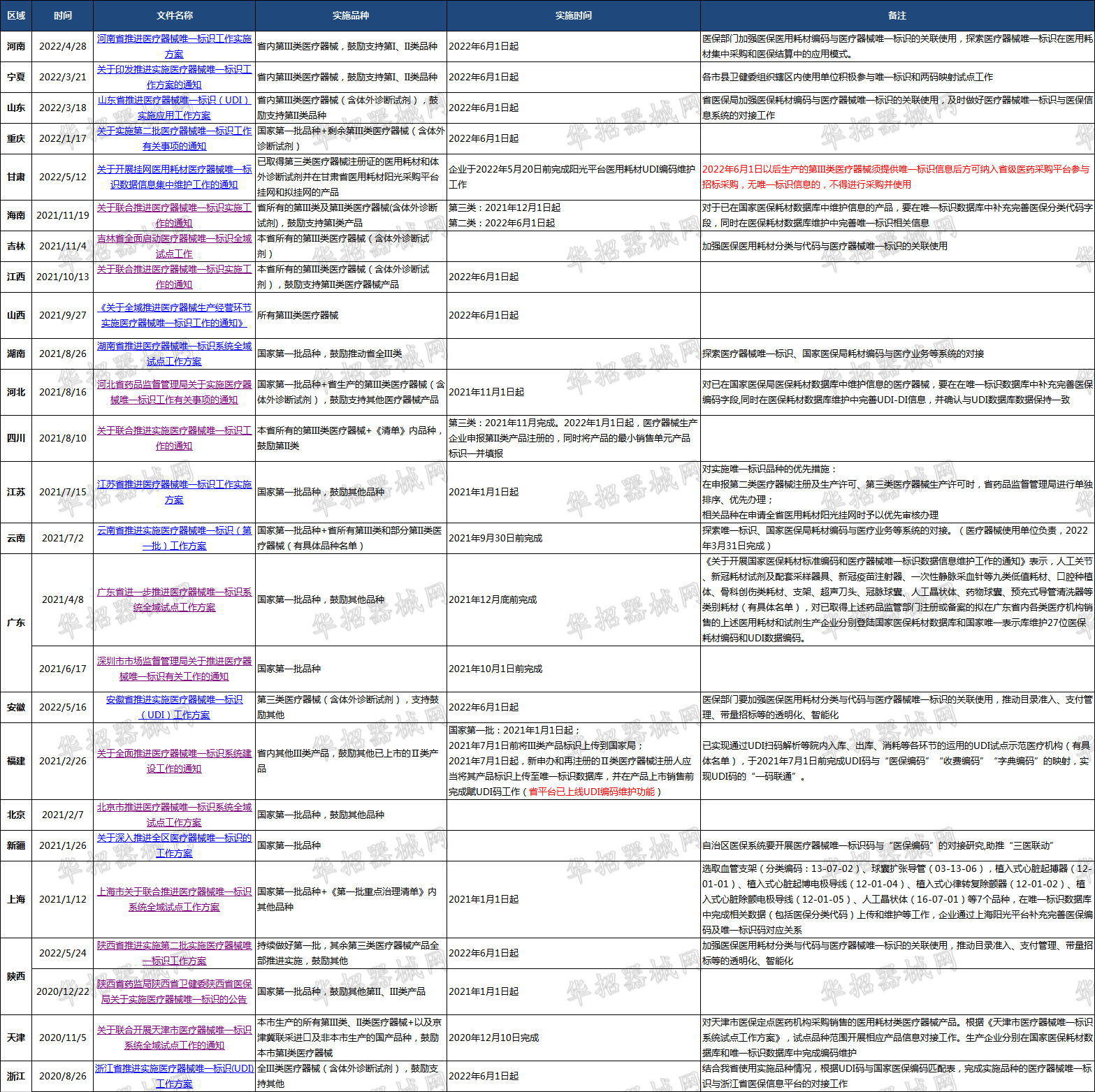
根据《国家药监局 国家卫生健康委 国家医保局关于做好第二批实施医疗器械唯一标识工作的公告》(2021年第114号 )要求,在第一批9大类69个品种的基础上,将其余第三类医疗器械(含体外诊断试剂)纳入第二批实施唯一标识范围,并自2022年6月1日起,生产的第三类医疗器械(含体外诊断试剂)应当具有医疗器械唯一标识。
现医疗器械唯一标识工作已经进入最后紧急实施阶段,多省积极发文响应,其中海南、四川、福建、云南等省已扩展到第二类医疗器械。
此外,福建、甘肃等省平台已上线UDI编码维护功能,要求相关企业登陆阳光采购平台维护医用耗材UDI编码,甘肃更是规定2022年6月1日以后生产的第III类医疗器械须提供唯一标识信息后方可纳入省平台参与招标采购,无唯一标识信息的,不得进行采购并使用。
另外,新版《医疗器械生产监督管理办法》已于2022年5月1日执行,其中对医疗器械唯一标识工作做出明确规定。医疗器械注册人、备案人、受托生产企业应当按照国家实施医疗器械唯一标识的有关要求,开展赋码、数据上传和维护更新。未按照国家实施医疗器械唯一标识的有关要求,组织开展赋码、数据上传和维护更新等工作的,由药品监督管理部门依职责责令限期改正;拒不改正的,处1万元以上5万元以下罚款;情节严重的,处5万元以上10万元以下罚款。